특집
소세포폐암의 표적 치료
- 배경
- 폐암은 암세포의 크기와 형태 등 병리조직학적 기준에 따라 소세포폐암과 비소세포폐암으로 구분된다. 소세포폐암은 세포 크기가 작아서 붙여진 이름으로, 비소세포폐암보다 치료가 어려운 것으로 알려져 있다. 수술보다는 항암치료에 의존하며, 1차 치료에 반응이 없을 경우 사용할 수 있는 치료제가 제한적이다. 또한, 2차 치료를 하더라도 약물 반응 기간이 짧아 생존율이 8개월을 넘기기 힘들어 치명적인 암으로 분류된다. 1차지료제로는 IMpower133 임상 결과에 따라, 티쎈트릭+카보플라틴+에토포시드 병용요법이 전체생존(OS) 중앙값은 12.3개월(95% CI, 10.8-15.9)을 보였으며, 환자의 1년 생존율은 대조군보다 13.5% 높은 51.7%를 기록해서 널리 사용되고 있다. 그것 외에는 그동안 몇가지 표적이 소세포 폐암에서도 연구되었으나 2019년 애브비가 항 DLL3 ADC인 로바-T(Rova-T)의 개발 실패로 소세포폐암에 있어 표적 치료제 개발은 좌절을 경험했었다.
- 동향
-
최근 소세포폐암에서 탈라타맙과 같은 이중특이성 T세포관여항체(Bispecific T-cell engager, 이중항체)의 가능성을 발견했다. 탈라타맙은 암세포와 면역세포 두 곳에서 발생한 항원을 인식하는 이중항체 신약으로, 암세포가 면역세포를 회피하려 해도 면역세포인 T세포를 암세포 앞으로 직접 끌고 가서 공격하도록 유도하는 약물이다.
탈라타맙은 소세포폐암 환자의 85~94%에서 발현되는 DLL3 단백질과 면역세포를 유도하는 CD3 수용체를 표적으로 한다. 최근 발표된 논문에서 세계 17개국 56개 기관에서 소세포폐암의 1차 치료에 실패한 환자 220명을 모집하여 무작위로 나누어 임상시험을 진행했다. FDA 가이드라인에 따라 탈라타맙을 10mg과 100mg으로 나누어 환자들에게 투여한 후 치료 반응과 부작용 등의 예후를 살폈다. 그 결과, 임상 효과 면에서 예후 개선과 부작용 감소에는 10mg을 2주 간격으로 투여하는 것이 환자에게 최적인 것으로 밝혀졌다. 추적 관찰 기간 동안 객관적 치료 반응이 나타난 환자 비율은 10mg 그룹이 40%로, 100mg 그룹의 32%보다 높았다. 무진행 생존기간 중앙값도 10mg 그룹이 4.9개월로 100mg 그룹의 3.9개월로 나타났다. 치료 후 9개월 차에 추산한 전체 생존율도 각각 68%(10mg 그룹)와 66%(100mg 그룹)로 소폭 차이를 보였다.
T세포를 활성화하는 치료 방법이기 때문에 과도하게 발현된 면역세포로 인한 ‘사이토카인 폭풍’ 발생 우려가 있는데, 10mg 그룹에서는 51%, 100mg 그룹에서는 61%에서 발생했다. 또한 식욕 감퇴, 발열 등 다른 부작용도 10mg 그룹에서 더 낮게 나타났다.
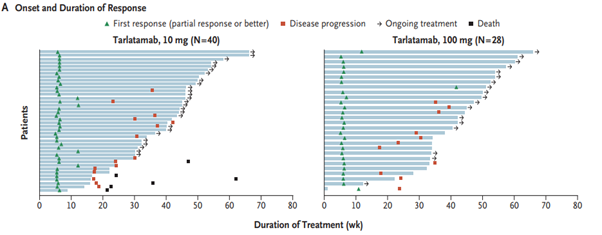
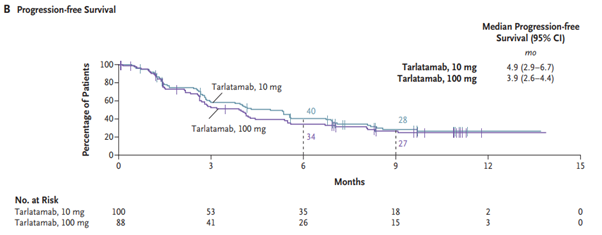
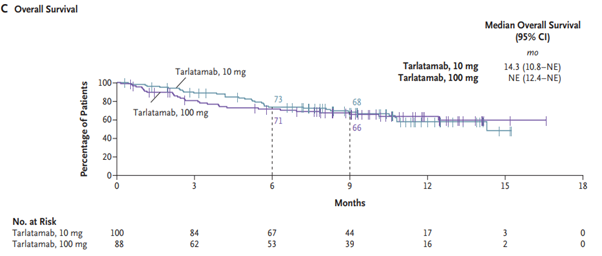
그림1. 소세포폐암의 탈라타맙 반응
그 외에도 최근에는 이피나타맙 데룩스테칸, B7-H3(또는 CD276) 표적 ADC에 대한 임상이 활발히 진행되고 있다. B7-H3 (CD276)은 B7 및 CD28 패밀리의 중요한 면역 체크포인트 구성원으로, 항원 제시 세포에서 유도된 B7-H3는 T 세포 기능 억제에 중요한 역할을 한다. 흑색종, 백혈병, 유방암, 폐암, 전립선암, 난소암, 췌장암, 결장 직장암 등 다양한 인간 악성 종양에서 B7-H3의 과발현이 여러 연구에 의해 증명되었고, 면역염색화학 진단을 통해 환자 종양 조직의 60~93%에서 B7-H3의 비정상적인 발현이 확인되고 있어 하나의 좋은 표적이 됨을 보여주었다.
다이이찌 산쿄 회사는 이약의 고형종양 환자를 대상으로 진행한 1/2상 연구에서 소세포폐암군의 3차 이상 차수의 치료에 대한 결과를 공개한 바 있다. 21명의 환자 중 11명(52.4%)이 객관적 반응을 보였으며, 반응 기간 중앙값은 5.9개월, 무진행 생존 중앙값은 5.6개월, 전체 생존 기간은 12.2개월이었다. 최근에는 이피나타맙 데룩스테칸, 3상 임상이 등록되어, 의사가 선택한 표준 치료법과 비교하여 소세포폐암 환자의 2차 치료에서의 효과를 비교 평가하게 된다.
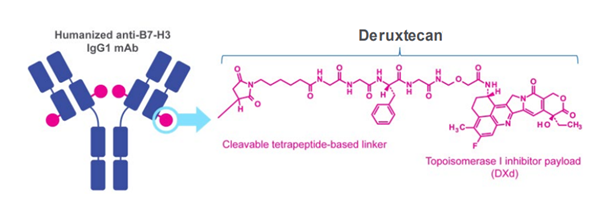
그림2. 이피나타맙 데룩스테칸 구조식
그 외에도 현재 개발중인 타깃으로는 TROP2, SEZ6 등이 있으며 아직 임상 초기 단계로 이에 대한 유용성을 평가하기는 아직 이른 단계라서 추후 결과를 지켜 보아야 한다.
이제 소세포폐암은 세포독성 항암과 면역항암치료를 넘어서 새로운 치료의 시대를 맞이하고있다. 우리가 고전적으로 알고 있던 표적치료제인 타이로신키나아제가 아닌 항체약물접합체 또는 이를 변형한 이중특이성 T세포관여항체가 그것으로 이제 환자에게 더 많은 희망을 줄 수 있게 되었다.
- Reference
-
- N Engl J Med 2023;389:2063-2075
- Mol Cancer Ther. 2022 Apr 1;21(4):635-646.
- Oncotarget. 2015;6:22496.
- Biochem Biophys Res Commun. 1995;216(1):382-9





